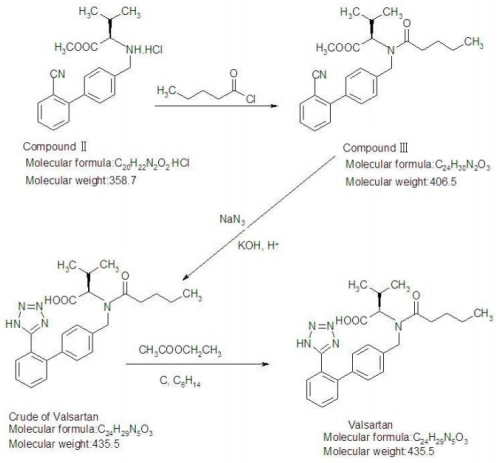
فالسارتان CAS 137862-53-4 فحص 98.0~102.0% API USP قياسي
Ruifu Chemical هي المورد الرئيسي لـ Valsartan (CAS: 137862 - 53 - 4) بجودة عالية، ويمكن أن تلبي معيار USP / EP. تقوم شركة Ruifu Chemical بتوريد واجهات برمجة التطبيقات والمواد الوسيطة الصيدلانية منذ أكثر من 15 عامًا.
يمكن أن توفر Ruifu Chemical التسليم في جميع أنحاء العالم والأسعار التنافسية والخدمة الممتازة.
شراء فالسارتان والوسائط ذات الصلة، يرجى الاتصال بنا عبر البريد الإلكتروني: alvin@ruifuchem.com
| الاسم الكيميائي | فالسارتان |
| المرادفات | N-فاليريل-N-[2'-(1H-تترازول-5-ييل) ثنائي الفينيل-4-يلميثيل]-L-فالين |
| رقم كاس | 137862-53-4 |
| حالة المخزون | في المخزون، يصل الإنتاج إلى طن |
| الصيغة الجزيئية | C24H29N5O3 |
| الوزن الجزيئي | 435.52 |
| نقطة الانصهار | 116.0 ~ 117.0 درجة مئوية |
| الكثافة | 1.212±0.06 جم/سم3 |
| الاستقرار | استرطابي |
| الذوبان | قابل للذوبان في الميثانول |
| شهادة توثيق البرامج وMSDS | متاح |
| الأصل | شنغهاي، الصين |
| فئات المنتجات | API (المكون الصيدلاني النشط) |
| العلامة التجارية | رويفو الكيميائية |
| عناصر الاختبار | المواصفات | النتائج |
| المظهر | الأبيض إلى مسحوق بلوري أبيض تقريبا | مسحوق بلوري أبيض |
| تحديد الهوية | ||
| IR | يجب أن يتوافق مع المعيار المرجعي | يتوافق |
| HPLC | يجب أن يتوافق مع المعيار المرجعي | يتوافق |
| الامتصاص (420 ملم) | ≥0.02% (420 نانومتر، C=0.05 جم/مل، L=1 سم) | 0.012% |
| الماء (بواسطة KF) | .001.00% | 0.20% |
| بقايا على الاشتعال | .10.10% | 0.06% |
| المعادن الثقيلة | .000.001% | <0.001% |
| المواد ذات الصلة | ||
| مجمع أ | .001.00% | 0.37% |
| مجمع ب | .20.20% | 0.02% |
| مجمع ج | .10.10% | غير قابل للاكتشاف |
| أي نجاسة فردية أخرى | .10.10% | 0.02% |
| مجموع الشوائب | ≥0.30% (باستثناء R-الأيزومر) | 0.07% |
| المذيبات المتبقية (GC) | ||
| الميثانول | ≥3000 جزء في المليون | 693 جزء في المليون |
| خلات الإيثيل | ≥5000 جزء في المليون | 3013 جزء في المليون |
| N، N - ثنائي ميثيل فورماميد | ≥880 جزء في المليون | غير قابل للاكتشاف |
| التولوين | ≥890 جزء في المليون | 8 جزء في المليون |
| طريقة الفحص / التحليل | 98.0~102.0% (محسوبة على اللامائية الأساس، المذيب-الأساس الحر) | 99.7% |
| معيار الاختبار | جامعة جنوب المحيط الهادئ 37 | يتوافق |
فالسارتان
C24H29N5O3 435.52
l-فالين، N-(1-أوكسوبينتيل)-N-[[2'-(1H-تترازول-5-yl)[1,1'-ثنائي الفينيل]-4-yl] ميثيل]-.
N-[p-(o-1H-تيترازول-5-يلفينيل)بنزيل]-N-فاليريل-ل-فالين [137862-53-4].
يحتوي فالسارتان على ما لا يقل عن 98.0 بالمائة ولا يزيد عن 102.0 بالمائة من C24H29N5O3، محسوبًا على الأساس اللامائي.
التعبئة والتغليف والتخزين-يحفظ في حاويات ضيقة، ويخزن في درجة حرارة 25، والرحلات المسموح بها بين 15 و30. يحفظ من الرطوبة والحرارة.
معايير USP المرجعية<11>-
يو إس بي فالسارتان آر إس
USP Valsartan مركب ذو صلة A RS
(R-N-فاليريل-N-([2'-(1H-تيترازول-5-يل) ثنائي الفين-4-يل] ميثيل) فالين.
C24H29N5O3 435.52
USP فالسارتان مركب ذو صلة B RS
(S-N-بوتيريل-N-([2'-(1H-تيترازول-5-ييل) ثنائي الفين-4-يل] ميثيل)-فالين.
C23H27N5O3 421.49
USP فالسارتان مركب ذو صلة C RS
(S-N-فاليريل-N-([2'-(1H-تيترازول-5-ييل) ثنائي الفين-4-يل] ميثيل)-إستر بنزيل فالين.
C31H35N5O3 525.64
تحديد الهوية-
ج: امتصاص الأشعة تحت الحمراء <197 م>.
ب: وقت الاحتفاظ بالذروة الرئيسية في اللوني لإعداد الفحص يتوافق مع ذلك الموجود في اللوني للإعداد القياسي، كما تم الحصول عليه في الفحص.
الامتصاصية-تحضير محلول 1 في 20 في الميثانول، وتحديد الامتصاصية عند 420 نانومتر. الامتصاصية مقسومة على طول المسار لا تزيد عن 0.02.
الماء، الطريقة الأولى<921>: لا يزيد عن 2.0%.
البقايا عند الاشتعال<281>: لا يزيد عن 0.1%.
المعادن الثقيلة، الطريقة الثانية<231>: 0.001%.
مركبات ذات صلة-
الاختبار 1 (الحد الأقصى للمركب المرتبط بالفالسارتان أ)-
المرحلة المتنقلة-تحضير خليط من n-الهكسان، 2-بروبانول، وحمض ثلاثي فلورو أسيتيك (85:15:0.1). قم بإجراء التعديلات إذا لزم الأمر (انظر ملاءمة النظام ضمن اللوني 621).
الحل القياسي-قم بإذابة كمية موزونة بدقة من مركب USP Valsartan المرتبط A RS في الطور المتنقل، وخففها كميًا وتدريجيًا إذا لزم الأمر، للحصول على محلول بتركيز معروف يبلغ حوالي 0.01 مجم لكل مليلتر.
حل ملاءمة النظام - قم بإذابة الكميات الموزونة بدقة من USP Valsartan RS والمركب المرتبط بـ USP Valsartan A RS في الطور المتنقل للحصول على محلول بتركيزات معروفة تبلغ حوالي 0.04 مجم لكل مليلتر لكل من المركب المرتبط بالفالسارتان والفالسارتان A.
محلول الاختبار-نقل حوالي 50 ملجم من فالسارتان، وزنه دقيقًا، إلى دورق حجمي سعة 50 مل، ثم أضف حوالي 40 مل من الطور المتحرك، وقم بالصوتنة لمدة 5 دقائق. تمييع مع الطور المحمول إلى حجم، وتخلط.
النظام الكروماتوغرافي (انظر الكروماتوغرافيا <621>)-تم تجهيز الكروماتوغرافيا السائلة بكاشف 230-نانومتر وعمود مقاس 4.6-مم × 25-سم يحتوي على تعبئة 5-ميكرومتر L40. معدل التدفق حوالي 0.8 مل في الدقيقة. تحليل كروماتوغرافي لمحلول ملاءمة النظام، وتسجيل استجابات الذروة وفقًا لتوجيهات الإجراء: الدقة، R، بين المركب المرتبط بفالسارتان A وفالسارتان لا تقل عن 2.0؛ والانحراف المعياري النسبي، المحدد من ذروة المركب المرتبط بالفالسارتان A، للحقن المتكرر لا يزيد عن 5%.
الإجراء-قم بحقن كميات متساوية (حوالي 10 ميكرولتر) من المحلول القياسي ومحلول الاختبار بشكل منفصل في الكروماتوجراف، وتسجيل المخططات اللونية، وقياس مناطق القمم الرئيسية. احسب النسبة المئوية للمركب المرتبط بالفالسارتان A في جزء فالسارتان المأخوذ بالصيغة:
100 (CS / CU) (RU / RS)
حيث CS هو التركيز، بالمجم لكل مليلتر، من مركب USP Valsartan المرتبط A RS في المحلول القياسي؛ CU هو تركيز فالسارتان، بالمجم لكل مليلتر، في محلول الاختبار؛ وru وrS هما الاستجابات القصوى للمركب المرتبط بالفالسارتان A الذي تم الحصول عليه من محلول الاختبار والحل القياسي، على التوالي: لم يتم العثور على أكثر من 1.0%.
الاختبار 2 (الحد الأقصى للمركب المرتبط بالفالسارتان ب، والمركب المرتبط بالفالسارتان ج، والمركبات الأخرى ذات الصلة)-
المرحلة المتنقلة-تابع وفقًا لتوجيهات الفحص.
الحل القياسي-قم بإذابة الكميات الموزونة بدقة من USP Valsartan RS، وUSP Valsartan ذو الصلة B RS، وUSP Valsartan ذو الصلة C RS في الطور المتنقل، وخففه كميًا وتدريجيًا إذا لزم الأمر، مع الطور المتحرك للحصول على محلول له تركيزات معروفة تبلغ حوالي 0.001 مجم من فالسارتان لكل مليلتر، و0.001 مجم من المركب المرتبط بالفالسارتان B لكل مليلتر، و 0.001 مجم من مركب فالسارتان C لكل مليلتر.
محلول الاختبار-نقل حوالي 50 مجم من فالسارتان، وزنه دقيقًا، إلى دورق حجمي سعة 100-مل، ثم يذاب في الطور المتحرك ويخففه حتى الحجم، ثم يخلط.
النظام الكروماتوغرافي (انظر اللوني<621>)-التحضير وفقًا لتوجيهات الفحص، باستثناء استخدام كاشف 225-نانومتر. تحليل كروماتوغرافي للمحلول القياسي، وتسجيل استجابات الذروة وفقًا لتوجيهات الإجراء: الدقة، R، بين المركب المرتبط بالفالسارتان B والفالسارتان لا تقل عن 1.8؛ لا يزيد الانحراف المعياري النسبي، المحدد من قمم المركب B المرتبط بالفالسارتان، عن الحقن المكررة عن 10.0%؛ والانحراف المعياري النسبي، المحدد من قمم فالسارتان، للحقن المتكرر لا يزيد عن 2.0%.
الإجراء-قم بحقن كميات متساوية (حوالي 10 ميكرولتر) من المحلول القياسي ومحلول الاختبار بشكل منفصل في الكروماتوجراف، وتسجيل المخططات اللونية، وقياس مناطق القمم الرئيسية. احسب النسبة المئوية للمركب المرتبط بالفالسارتان B والمركب المرتبط بالفالسارتان C في جزء فالسارتان المأخوذ بواسطة الصيغة:
100(CS/CU)(ري/RS)
حيث CS هو التركيز، بالمجم لكل مليلتر، من مركب USP Valsartan المرتبط RS المناسب في المحلول القياسي؛ CU هو تركيز فالسارتان، بالمجم لكل مليلتر، في محلول الاختبار؛ ri هو استجابة الذروة للشوائب التي تم الحصول عليها من محلول الاختبار؛ و rS هي استجابة الذروة للمركب المناسب المرتبط بالفالسارتان والذي تم الحصول عليه من المحلول القياسي. احسب النسبة المئوية لكل شوائب أخرى في جزء فالسارتان المأخوذ بنفس الصيغة، حيث CS هو التركيز، بالملجم لكل مل، من USP Valsartan RS في المحلول القياسي؛ rS هي استجابة الذروة لفالسارتان التي تم الحصول عليها من المحلول القياسي؛ والمصطلحات الأخرى كما هي محددة أعلاه: تم العثور على ما لا يزيد عن 0.2% من المركب B المرتبط بالفالسارتان؛ تم العثور على ما لا يزيد عن 0.1% من المركب C المرتبط بالفالسارتان؛ تم العثور على ما لا يزيد عن 0.1% من أي شوائب فردية أخرى، باستثناء المركب A المرتبط بالفالسارتان؛ ولم يتم العثور على أكثر من 0.3% من إجمالي الشوائب، باستثناء المركب A المرتبط بالفالسارتان.
مقايسة-
المرحلة المتنقلة-تحضير خليط من الماء والأسيتونيتريل وحمض الأسيتيك الجليدي (500:500:1) تمت تصفيته وطرد الغاز منه. قم بإجراء التعديلات إذا لزم الأمر (انظر ملاءمة النظام ضمن اللوني 621).
التحضير القياسي-قم بإذابة كمية موزونة بدقة من USP Valsartan RS في الطور المتحرك، وخففها كميًا وتدريجيًا إذا لزم الأمر، مع الطور المتحرك للحصول على محلول له تركيز معروف يبلغ حوالي 0.5 مجم لكل مليلتر.
تحضير المقايسة-نقل حوالي 50 ملجم من فالسارتان، وزنه دقيقًا، إلى دورق حجمي سعة 100-مل، ثم يذاب في الطور المتحرك ويخففه للحصول على الحجم، ثم يخلط.
النظام الكروماتوغرافي (انظر الكروماتوغرافيا <621>)-تم تجهيز الكروماتوغرافيا السائلة بكاشف 273-نانومتر وعمود مقاس 3.0-مم × 12.5-سم يحتوي على تعبئة 5-ميكرومتر L1. معدل التدفق حوالي 0.4 مل في الدقيقة. كروماتوغراف الإعداد القياسي، وتسجيل استجابات الذروة وفقًا لتوجيهات الإجراء: الانحراف المعياري النسبي للحقن المتماثل لا يزيد عن 2.0%.
الإجراء-قم بحقن كميات متساوية (حوالي 10 ميكرولتر) من الإعداد القياسي وإعداد الفحص بشكل منفصل في الكروماتوغرافي، وتسجيل المخططات اللونية، وقياس مناطق القمم الرئيسية. احسب الكمية بالملغ من C24H29N5O3 في جزء فالسارتان المأخوذ بالصيغة:
100C (رو / آر إس)
حيث C هو التركيز، بالمجم لكل مليلتر، من USP Valsartan RS في المستحضر القياسي؛ وru وrS هي الاستجابات الذروة التي تم الحصول عليها من إعداد الفحص والإعداد القياسي، على التوالي.
الحزمة: زجاجة ، كيس رقائق الألومنيوم ، 25 كجم/أسطوانة من الورق المقوى ، أو وفقًا لمتطلبات العميل.
حالة التخزين: أبقِ الحاوية مغلقة بإحكام وقم بتخزينها في مستودع بارد وجاف (2 ~ 8 درجة مئوية) وجيد التهوية بعيدًا عن المواد غير المتوافقة. حماية من الضوء والرطوبة.
الشحن: التسليم إلى جميع أنحاء العالم عن طريق الجو، عن طريق FedEx / DHL Express. توفير تسليم سريع وموثوق.

رموز الخطر Xi - مهيج
رموز المخاطر
36/37/38 - مهيجة للعيون والجهاز التنفسي والجلد.
وصف السلامة
س26 - في حالة ملامسة العينين، اشطفهما فورًا بالكثير من الماء واطلب المشورة الطبية.
س37/39 - ارتداء القفازات المناسبة وحماية العين / الوجه
دبليو جي كيه ألمانيا 3
آرتيكس YV9455000
رمز النظام المنسق 2933990099
تعتبر شركة Shanghai Ruifu Chemical Co., Ltd. الشركة الرائدة في تصنيع وتوريد عقار فالسارتان (CAS: 137862-53-4) بجودة عالية. فالسارتان هو مضاد لمستقبلات الأنجيوتنسين II AT1 غير الببتيد، وهو خافض لضغط الدم، وله القدرة على علاج ارتفاع ضغط الدم وأبحاث قصور القلب.
تعتبر التأثيرات الخافضة لضغط الدم لفالسارتان أقوى من تأثيرات إنالابريل، وهي مناسبة لعلاج ارتفاع ضغط الدم، وارتفاع ضغط الدم الأولي الخفيف إلى المتوسط، وخاصة ارتفاع ضغط الدم الثانوي الناجم عن تلف الكلى. يمكن أن يقلل بشكل كبير من بروتينية مرضى ارتفاع ضغط الدم الذين يعانون من مرض السكري أو وظائف الكبد الطبيعية، ويمكن أن يعزز حمض اليوريك والصوديوم البولي لحماية الكلى. فالسارتان مناسب أيضًا لتقليل معدل الوفيات القلبية الوعائية للمرضى المعرضين لمخاطر عالية (فشل البطين الأيسر أو خلل وظيفي) بعد الإصابة بنوبة قلبية.