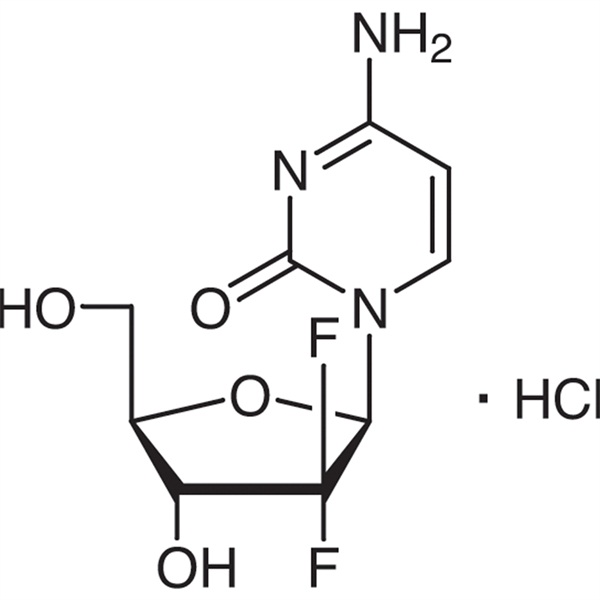
جيمسيتابين هيدروكلوريد CAS 122111-03-9 معيار API USP35
Ruifu Chemical هي الشركة الرائدة في تصنيع Gemcitabine Hydroكلورide (CAS: 122111-03-9) بجودة عالية وإنتاج تجاري. يمكن أن توفر Ruifu Chemical خدمة التوصيل في جميع أنحاء العالم والأسعار التنافسية والخدمة الممتازة والكميات الصغيرة والكبيرة المتاحة. شراء جيمسيتابين هيدروكلوريد، يرجى الاتصال: alvin@ruifuchem.com
| الاسم الكيميائي | جيمسيتابين هيدروكلوريد |
| المرادفات | جيمسيتابين حمض الهيدروكلوريك. 2'-ديوكسي-2',2'-ديفلوروسيتيدين هيدروكلوريد؛ dFdC; dFdCyd; جمزار؛ LY188011 هيدروكلوريد؛ جيمسيتيرا؛ جيمسار |
| رقم كاس | 122111-03-9 |
| CAS ذات الصلة | 95058-81-4 - قاعدة مجانية |
| حالة المخزون | متوفر في المخزون، القدرة الإنتاجية 5 طن |
| الصيغة الجزيئية | C9H12ClF2N3O4 |
| الوزن الجزيئي | 299.66 |
| نقطة الانصهار | > 250 درجة مئوية |
| حالة الشحن | تحت درجة الحرارة المحيطة |
| شهادة توثيق البرامج وMSDS | متاح |
| الأصل | شنغهاي، الصين |
| العلامة التجارية | رويفو الكيميائية |
| البند | المواصفات | النتائج |
| المظهر | مسحوق بلوري أبيض، عديم الرائحة | يتوافق |
| الذوبان | قابل للذوبان في الماء، قابل للذوبان بشكل طفيف في الميثانول، غير قابلة للذوبان عمليا في الأسيتون | يتوافق |
| تحديد الهوية IR | يجب أن يكون طيف الأشعة تحت الحمراء متوافقًا مع أن المعيار المرجعي | يتوافق |
| تحديد كلوريد | إيجابي. يفي بمتطلبات اختبارات الكلوريد | يتوافق |
| ظهور الحل | الحل S واضح وليس أكثر كثافة الملونة من الحل المرجعي BY7 | يتوافق |
| pH | 2.0 ~ 3.0 | 2.6 |
| الدوران النوعي [α]20/د | +43.0 درجة إلى +50.0 درجة | +47.5 درجة |
| المعادن الثقيلة (الرصاص) | ≥10 جزء في المليون | <10 جزء في المليون |
| خسارة في التجفيف | .001.00% | 0.3% |
| بقايا على الاشتعال | .10.10% | 0.03% |
| المواد ذات الصلة | ||
| السيتوزين | .10.10% | 0.01% |
| α-أيزومر | .10.10% | 0.01% |
| أي نجاسة أخرى | .10.10% | 0.04% |
| مجموع الشوائب | .20.20% | 0.1% |
| المذيبات المتبقية | ||
| الميثانول | .30.30% | لم يتم الكشف عنها |
| التولوين | .0.01% | لم يتم الكشف عنها |
| ثنائي كلورو ميثان | .0.01% | لم يتم الكشف عنها |
| الأسيتون | .50.50% | 0.1% |
| فحص | 97.5%~101.5% (محسوب على القاعدة المجففة) | 99.9% |
| الاستنتاج | يتوافق مع معيار USP35 | |
الحزمة: زجاجة ، كيس رقائق الألومنيوم ، 25 كجم/أسطوانة من الورق المقوى ، أو وفقًا لمتطلبات العميل.
حالة التخزين: أبقِ الحاوية مغلقة بإحكام وقم بتخزينها في مستودع بارد وجاف وجيد التهوية بعيدًا عن المواد غير المتوافقة. تجنب التعرض لأشعة الشمس المباشرة والرطوبة والحرارة الزائدة.
الشحن: التسليم إلى جميع أنحاء العالم عن طريق الجو، عن طريق FedEx / DHL Express. توفير تسليم سريع وموثوق.

رموز المخاطر R21 - ضارة عند ملامستها للجلد
ر36/38 - مهيجة للعيون والجلد.
ر46 - قد يسبب ضررا وراثيا وراثيا
آر 62 - خطر محتمل لضعف الخصوبة
ر63 - خطر محتمل لإلحاق الأذى بالطفل الذي لم يولد بعد
وصف السلامة S25 - تجنب ملامسة العينين.
س26 - في حالة ملامسة العينين، اشطفهما فورًا بالكثير من الماء واطلب المشورة الطبية.
س36/37 - ارتداء الملابس الواقية والقفازات المناسبة.
س53 - تجنب التعرض - الحصول على تعليمات خاصة قبل الاستخدام.
دبليو جي كيه ألمانيا 3
آرتيكس HA3840000
رمز النظام المنسق 2942000000
جيمسيتابين هيدروكلوريد (CAS: 122111-03-9) هو دواء اصطناعي جديد من ثنائي فلورو نيوكليوسيد مضاد للأيض ومضاد للأورام. تم بحثه وتطويره بواسطة شركة Eli Lilly and Company وتمت الموافقة على إدراجه في جنوب أفريقيا والسويد وهولندا وأستراليا وبلدان أخرى في عام 1995. وقد وافقت عليه إدارة الغذاء والدواء الأمريكية (FDA) باعتباره العلاج الخطي الأول للعلاج السريري لسرطان الرئة ذو الخلايا غير الصغيرة وسرطان البنكرياس.
في السنوات الأخيرة، أصبحت أدوية جديدة مثل جيمسيتابين، باكليتاكسيل، دوسيتاكسيل، فينوربين أدوية فعالة لعلاج سرطان الرئة ذو الخلايا غير الصغيرة (المختصر NSCLC). بالمقارنة مع أدوية العلاج الكيميائي التقليدية، تتمتع هذه الأدوية بمزايا التأثير العلاجي العالي والسمية المنخفضة. جيمسيتابين هيدروكلوريد هو جيل جديد من الأدوية المضادة للأيضات ونوع من الأدوية الخاصة لدورة الخلية، ويلعب دورًا رئيسيًا في مرحلة تخليق الحمض النووي، أي المرحلة S للخلايا. في ظل ظروف معينة، يمكن لهذا الدواء أن يمنع تطور الخلايا من المرحلة G1 إلى المرحلة S، ويكون له نشاط قوي مضاد للسرطان غير سرطان الرئة ذو الخلايا الصغيرة (NSCLC). أظهرت الدراسات الأجنبية أن كفاءة العلاج الفردي لـ NSCLC باستخدام جيمسيتابين هيدروكلوريد فقط تبلغ حوالي 18% إلى 35%، في حين أن الجمع بين العلاج مع السيسبلاتين فإن كفاءة NSCLC تبلغ 41.7%. في سرطان الرئة غير صغير الخلايا المتقدم، يبلغ المعدل الفعال للكاربوبلاتين 16%، وهو مشابه للسيسبلاتين، لكن له سمية منخفضة، خاصة بالنسبة للتفاعلات المعدية المعوية، وتثبيط نخاع العظم والتفاعل السام للكلى ونهايات الأعصاب. بالاشتراك مع الكاربوبلاتين، كلاهما لهما تنسيق متبادل وتأثير إضافي، ويمكنهما إنتاج تأثيرات علاجية أعلى.
جيمسيتابين هيدروكلوريد
C9H11F2N3O4 · حمض الهيدروكلوريك 299.66
سيتيدين، 2'-ديوكسي-2'،2'-ديفلورو-، مونوهيدروكلوريد.
2'-ديوكسي-2',2'-ثنائي فلوروسيتيدين مونوهيدروكلوريد ( β-أيزومر) [122111-03-9].
» يحتوي جيمسيتابين هيدروكلوريد على ما لا يقل عن 97.5 بالمائة ولا يزيد عن 101.5 بالمائة من C9H11F2N3O4·HCl، محسوبًا على أساس الحالة الحالية.
[تحذير-جيمسيتابين هيدروكلوريد هو عامل قوي سام للخلايا. وينبغي الحرص الشديد على منع استنشاق الجزيئات وتعريض الجلد لها.]
التعبئة والتغليف والتخزين-الحفظ في حاويات ضيقة.
وضع العلامات-عندما يكون المنتج مخصصًا للاستخدام في تحضير أشكال الجرعات القابلة للحقن، فإن الملصق يشير إلى أنه معقم أو يجب أن يخضع لمزيد من المعالجة أثناء تحضير أشكال الجرعات القابلة للحقن.
معايير USP المرجعية<11>-
USP السيتوزين RS
USP الذيفان الداخلي RS
USP جيمسيتابين هيدروكلوريد RS
تحديد الهوية-
ج: امتصاص الأشعة تحت الحمراء <197 ك>.
ب: مطابق لمتطلبات اختبارات الكلوريد<191>.
الدوران النوعي<781S>: بين +43 و+50، عند 20.
محلول الاختبار: 10 ملغ لكل مل.
الرقم الهيدروجيني <791>: بين 2.0 و 3.0 في محلول يحتوي على 10 ملغ لكل مليلتر.
البقايا عند الاشتعال<281>: لا يزيد عن 0.1%.
المعادن الثقيلة، الطريقة الأولى<231>: 0.001%.
النقاء الكروماتوغرافي-
الحل أ- تابع وفقًا لتوجيهات المرحلة المتنقلة في الفحص.
الحل ب-تحضير الميثانول المصفى ومنزوع الغاز.
الطور المتحرك-استخدم خليطًا متغيرًا من المحلول A والمحلول B وفقًا لتوجيهات النظام الكروماتوغرافي. قم بإجراء التعديلات، إذا لزم الأمر (انظر ملاءمة النظام ضمن اللوني 621).
حل ملاءمة النظام - تابع وفقًا لتوجيهات الفحص.
الحل القياسي-قم بإذابة كمية موزونة بدقة من USP Gemcitabine Hydroكلورide RS وUSP Cytosine RS في الماء، وخففها كميًا وتدريجيًا إذا لزم الأمر، للحصول على محلول بتركيز معروف يبلغ حوالي 2 ميكروغرام لكل مل من كل منهما.
محلول الاختبار-نقل حوالي 50 ملجم من جيمسيتابين هيدروكلوريد، وزنه دقيقًا، إلى دورق حجمي سعة 25 مل، ثم يذوب في الماء ويخففه للحصول على الحجم، ثم يخلط.
النظام الكروماتوغرافي (انظر اللوني 621)-تابع وفقًا لتوجيهات الفحص. تتم برمجة الكروماتوغراف على النحو التالي.
الوقت (بالدقائق) الحل أ (%) الحل ب (%) الشطف
0–8 97 3 إسقراطي
8–13 97®50 3®50 التدرج الخطي
13-20 50 50 إسقراطي
20–25 50®97 50®3 إعادة الموازنة
قم بتصوير محلول ملاءمة النظام، وقم بتسجيل استجابات الذروة وفقًا لتوجيهات الإجراء: أوقات الاستبقاء النسبية هي حوالي 0.5 لجيمسيتابين -أنومر و1.0 لجيمسيتابين؛ الدقة R بين جيمسيتابين -أنومر وجيمسيتابين لا تقل عن 8.0؛ وعامل المخلفات للجيمسيتابين لا يزيد عن 1.5. تحليل كروماتوغرافي للحل القياسي، وتسجيل استجابات الذروة وفقًا لتوجيهات الإجراء: أوقات الاستبقاء النسبية هي حوالي 0.1 للسيتوزين و1.0 للجيمسيتابين؛ لا يزيد الانحراف المعياري النسبي للحقن المكرر عن 2.0%.
الإجراء-قم بحقن حجم (حوالي 20 ميكرولتر) من المحلول القياسي ومحلول الاختبار بشكل منفصل في الكروماتوغراف، وتسجيل المخطط اللوني، وقياس جميع استجابات الذروة. احسب النسبة المئوية للسيتوزين في جزء جيمسيتابين المأخوذ بالصيغة:
2.5(سم مكعب/ث)(rt/rs)
حيث Cc هو تركيز USP Cytosine RS في المحلول القياسي، بالميكروجرام لكل مليلتر؛ W هو وزن جيمسيتابين المأخوذ بالملغ. rt هو استجابة الذروة للسيتوزين في محلول الاختبار؛ و rs هي استجابة السيتوزين في المحلول القياسي: لم يتم العثور على أكثر من 0.1٪ من السيتوزين. احسب النسبة المئوية لكل شوائب غير السيتوزين في جزء جيمسيتابين المأخوذ بالصيغة:
2.5(Cs/W)(ري/RS)
حيث Cs هو تركيز USP Gemcitabine هيدروكلوريد RS في المحلول القياسي، بالميكروجرام لكل مليلتر؛ W هو وزن جيمسيتابين المأخوذ بالملغ. ri هو استجابة الذروة لكل شوائب في محلول الاختبار؛ و rs هي الاستجابة الناتجة عن جيمسيتابين في المحلول القياسي: لم يتم العثور على أكثر من 0.1% من جيمسيتابين -أنومر أو أي شوائب فردية أخرى؛ ومجموع الشوائب لا يزيد عن 0.2%. استبعاد من مجموع كافة الشوائب أي قمم تكون أقل من الحد الكمي (0.02%).
متطلبات أخرى-حيث يشير الملصق إلى أن جيمسيتابين هيدروكلوريد معقم، فإنه يلبي متطلبات السموم الداخلية البكتيرية والعقم بموجب جيمسيتابين للحقن. عندما تشير الملصق إلى أن جيمسيتابين هيدروكلوريد يجب أن يخضع لمزيد من المعالجة أثناء تحضير أشكال الجرعات القابلة للحقن، فإنه يلبي متطلبات السموم الداخلية البكتيرية بموجب جيمسيتابين للحقن.
مقايسة-
الطور المتحرك-قم بتحضير محلول مُرشح ومنزوع الغازات يحتوي على 13.8 جم من فوسفات الصوديوم أحادي القاعدة و2.5 مل من حمض الفوسفوريك في 1000 مل من الماء. [ملاحظة-درجة الحموضة لهذا المحلول تتراوح بين 2.4 و2.6. ]
محلول ملائم للنظام-نقل حوالي 10 ملغ من جيمسيتابين هيدروكلوريد إلى قارورة صغيرة، أضف 4 مل من محلول يحتوي على 168 ملغ من هيدروكسيد البوتاسيوم لكل مل من الميثانول، قم بتغطية الغطاء بإحكام، ثم يصوتن. سخنه عند درجة حرارة 55 لمدة 6 إلى 16 ساعة، واتركه ليبرد، ثم انقل المحتويات إلى دورق حجمي سعة 100-مل مع عمليات غسل متتالية بحمض الفوسفوريك 1% (حجم/حجم). تمييع مع 1٪ حمض الفوسفوريك إلى الحجم، وتخلط. [ملاحظة-يحتوي هذا المحلول على حوالي 0.02 مجم لكل مليلتر من جيمسيتابين α-أنومر.]
التحضير القياسي-قم بإذابة كمية موزونة بدقة من USP Gemcitabine هيدروكلوريد RS في الماء، وخففها كميًا، وتدريجيًا إذا لزم الأمر، مع الماء للحصول على محلول بتركيز معروف يبلغ حوالي 0.1 مجم لكل مليلتر.
تحضير المقايسة-نقل حوالي 20 ملغ من جيمسيتابين هيدروكلوريد، وزنه دقيق، إلى دورق حجمي سعة 200-مل، ثم يذوب في الماء ويخففه بالماء حتى الحجم، ثم يخلط.
النظام الكروماتوغرافي (انظر الكروماتوغرافيا <621>)-تم تجهيز الكروماتوغرافيا السائلة بكاشف 275-نانومتر وعمود مقاس 4.6-مم × 25-سم يحتوي على تعبئة 5-ميكرومتر L7. معدل التدفق حوالي 1.2 مل في الدقيقة. قم بتصوير محلول ملاءمة النظام، وقم بتسجيل استجابات الذروة وفقًا لتوجيهات الإجراء: الدقة، R، بين جيمسيتابين -أنومر وجيمسيتابين لا تقل عن 8.0؛ وعامل المخلفات المحدد من جيمسيتابين لا يزيد عن 1.5. كروماتوغراف الإعداد القياسي، وتسجيل استجابات الذروة وفقًا لتوجيهات الإجراء: الانحراف المعياري النسبي للحقن المتماثل لا يزيد عن 1.0%.
الإجراء-قم بحقن كميات متساوية (حوالي 20 ميكرولتر) من الإعداد القياسي وإعداد المقايسة بشكل منفصل في الكروماتوغرافي، وتسجيل المخططات الاستشرابية، وقياس الاستجابات للقمم الرئيسية. احسب الكمية بالملغ من C9H11F2N3O4·HCl في جزء هيدروكلوريد جيمسيتابين المأخوذ بالصيغة:
200C (رو / آر إس)
حيث C هو التركيز، بالمجم لكل مليلتر، من USP Gemcitabine هيدروكلوريد RS في المستحضر القياسي؛ وru وrS هي الاستجابات الذروة التي تم الحصول عليها من إعداد الفحص والإعداد القياسي، على التوالي.