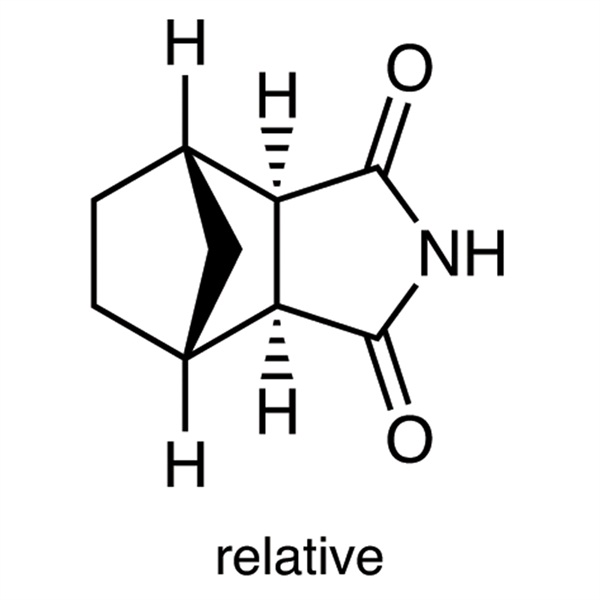
لوراسيدون هيدروكلوريد وسيط CAS 14805-29-9 نقاء ≥99.0% (HPLC)
| الاسم الكيميائي | (3aR,4S,7R,7aS)-rel-هيكساهيدرو-4,7-ميثانو-1H-إيزوإندول-1,3(2H)-ديون |
| المرادفات | إكسو-2,3-نوربورنانيديكاربوكسيميد؛ لوراسيدون هيدروكلوريد وسيط |
| رقم كاس | 14805-29-9 |
| حالة المخزون | في المخزون، يصل الإنتاج إلى طن |
| الصيغة الجزيئية | C9H11NO2 |
| الوزن الجزيئي | 165.19 |
| نقطة الانصهار | 150.0 ~ 154.0 درجة مئوية |
| الكثافة | 1.285 |
| حالة الشحن | يتم شحنه تحت درجة الحرارة المحيطة باعتباره مادة كيميائية غير-خطرة |
| شهادة توثيق البرامج وMSDS | متاح |
| مكان المنشأ | شنغهاي، الصين |
| العلامة التجارية | رويفو الكيميائية |
| البند | المواصفات |
| المظهر | الأبيض إلى مسحوق أبيض تقريبا |
| نقطة الانصهار | 150.0 ~ 154.0 درجة مئوية |
| التفريق | ح-الرنين المغناطيسي النووي |
| مجمع ذات الصلة | .50.50% |
| إندو أيزومر | .150.15% |
| النجاسة أ | ≥0.10% (3aR,4S,7R,7aS) 4,7-ميثانو-1H-إيزوإندول-1,3(2H)-ديون |
| ماكس. شوائب واحدة | .30.30% |
| إجمالي الشوائب | .001.00% |
| محتوى الماء | .001.00% |
| المعادن الثقيلة | ≥20 جزء في المليون |
| النقاء / طريقة التحليل | ≥99.0% ([هبلك]) |
| معيار الاختبار | معيار المؤسسة |
| الاستخدام | لوراسيدون هيدروكلوريد (CAS 367514-88-3) متوسط |
الحزمة: زجاجة مفلورة، كيس رقائق الألومنيوم، 25 كجم/أسطوانة من الورق المقوى، أو وفقًا لمتطلبات العميل.
حالة التخزين: أبقِ الحاوية مغلقة بإحكام وقم بتخزينها في مستودع بارد وجاف وجيد التهوية بعيدًا عن المواد غير المتوافقة. حماية من الضوء والرطوبة.
الشحن: التسليم إلى جميع أنحاء العالم عن طريق الجو، عن طريق FedEx / DHL Express. توفير تسليم سريع وموثوق.

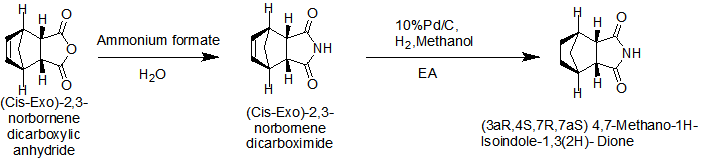
هي الشركة الرائدة في تصنيع وتوريد (3aR,4S,7R,7aS)-rel-Hexahydro-4,7-methano-1H-isoindole-1,3(2H)-dione (CAS 14805-29-9) بجودة عالية وإنتاج تجاري. ذلك هو مادة وسيطة عادة في تركيب هيدروكلوريد لوراسيدون (CAS 367514-88-3) في علاج الفصام.
تمت الموافقة على لوراسيدون من قبل إدارة الغذاء والدواء الأمريكية في عام 2010 لعلاج مرض انفصام الشخصية وفي عام 2013 لعلاج نوبات الاكتئاب المرتبطة بالاضطراب ثنائي القطب. لوراسيدون هو مادة يتم تناولها عن طريق الفم وتنتمي إلى فئة الأدوية المضادة للذهان غير التقليدية (AAPD). وقد حصل على موافقة وكالة الأدوية الأوروبية في عام 2014 لعلاج مرض انفصام الشخصية. تم إطلاق Lurasidone أيضًا في عدد من البلدان خارج الولايات المتحدة والاتحاد الأوروبي، بما في ذلك كندا، حيث تمت الموافقة عليه لكلا المؤشرين. يتم إنتاجه من خلال عملية كيميائية متعددة الخطوات.